গ্যালভানিক কোষ এবং ব্যাটারি - ডিভাইস, অপারেশন নীতি, প্রকার
বৈদ্যুতিক শক্তির কম শক্তি উৎস
গ্যালভানিক কোষ এবং ব্যাটারিগুলি বহনযোগ্য বৈদ্যুতিক এবং রেডিও সরঞ্জামগুলিকে পাওয়ার জন্য ব্যবহৃত হয়।
গ্যালভানিক কোষ - এগুলি এককালীন ক্রিয়াগুলির উত্স, accumulators - পুনরায় ব্যবহারযোগ্য কর্ম উত্স।

সহজতম গ্যালভানিক উপাদান
সবচেয়ে সহজ উপাদানটি দুটি স্ট্রিপ দিয়ে তৈরি করা যেতে পারে: তামা এবং দস্তা জলে ডুবিয়ে সালফিউরিক অ্যাসিডের সাথে সামান্য অম্লীয়। যদি দস্তা যথেষ্ট বিশুদ্ধ হয় কোন স্থানীয় প্রতিক্রিয়া না থাকে, তাহলে তামা এবং দস্তা একত্র না হওয়া পর্যন্ত কোন লক্ষণীয় পরিবর্তন ঘটবে না।
যাইহোক, স্ট্রিপগুলির একটি ভিন্ন সম্ভাবনা রয়েছে, একটি অন্যটির সাথে সাপেক্ষে এবং একটি তার দ্বারা সংযুক্ত হলে, প্রদর্শিত হবে বিদ্যুৎ… এই ক্রিয়া দ্বারা দস্তার ফালা ধীরে ধীরে দ্রবীভূত হবে এবং তামার ইলেক্ট্রোডের কাছে গ্যাসের বুদবুদ তৈরি হবে, তার পৃষ্ঠে সংগ্রহ করবে। এই গ্যাস ইলেক্ট্রোলাইট দ্বারা উত্পন্ন হাইড্রোজেন। বৈদ্যুতিক প্রবাহ তার বরাবর তামার স্ট্রিপ থেকে জিঙ্ক স্ট্রিপে প্রবাহিত হয় এবং তা থেকে ইলেক্ট্রোলাইটের মাধ্যমে তামায় ফিরে আসে।
ধীরে ধীরে, ইলেক্ট্রোলাইটের সালফিউরিক অ্যাসিড জিঙ্ক ইলেক্ট্রোডের দ্রবীভূত অংশ থেকে গঠিত জিঙ্ক সালফেট দ্বারা প্রতিস্থাপিত হয়। এতে কোষের ভোল্টেজ কমে যায়। যাইহোক, তামার উপর গ্যাস বুদবুদ গঠনের কারণে আরও বেশি ভোল্টেজ ড্রপ হয়। উভয় ক্রিয়াই 'মেরুকরণ' ঘটায়। এই জাতীয় আইটেমগুলির প্রায় কোনও ব্যবহারিক মূল্য নেই।
গ্যালভানিক কোষের গুরুত্বপূর্ণ পরামিতি
গ্যালভানিক কোষ দ্বারা প্রদত্ত ভোল্টেজের মাত্রা শুধুমাত্র তাদের প্রকার এবং ডিভাইসের উপর নির্ভর করে, অর্থাৎ, ইলেক্ট্রোডের উপাদান এবং ইলেক্ট্রোলাইটের রাসায়নিক গঠনের উপর, কিন্তু কোষের আকার এবং আকারের উপর নির্ভর করে না।
একটি গ্যালভানিক কোষ যে বিদ্যুৎ সরবরাহ করতে পারে তা তার অভ্যন্তরীণ প্রতিরোধের দ্বারা সীমাবদ্ধ।
গ্যালভানিক কোষের একটি অত্যন্ত গুরুত্বপূর্ণ বৈশিষ্ট্য বৈদ্যুতিক ক্ষমতা… বৈদ্যুতিক ক্ষমতা মানে একটি গ্যালভানিক বা স্টোরেজ সেল তার ক্রিয়াকলাপ জুড়ে, অর্থাৎ চূড়ান্ত নিষ্কাশনের শুরু পর্যন্ত যে পরিমাণ বিদ্যুৎ সরবরাহ করতে সক্ষম।
কোষ দ্বারা প্রদত্ত ক্ষমতা স্রাব কারেন্টের শক্তিকে গুণ করে, অ্যাম্পিয়ারে প্রকাশ করে, পূর্ণ স্রাবের শুরু পর্যন্ত সেলটি যে সময় থেকে নিঃসৃত হয়েছিল সেই সময়ের দ্বারা নির্ধারিত হয়। অতএব, ক্ষমতা সর্বদা অ্যাম্পিয়ার-আওয়ারে (আহ) প্রকাশ করা হয়।

কোষের ক্ষমতার মান দ্বারা, সম্পূর্ণ স্রাব শুরু হওয়ার আগে এটি কত ঘন্টা কাজ করবে তা আগেই নির্ধারণ করা সম্ভব। এটি করার জন্য, আপনাকে এই উপাদানটির জন্য অনুমোদিত স্রাব বর্তমানের শক্তি দ্বারা ক্ষমতা ভাগ করতে হবে।
তবে, ক্ষমতা কঠোরভাবে ধ্রুবক নয়। এটি উপাদানটির অপারেটিং অবস্থার (মোড) এবং চূড়ান্ত স্রাব ভোল্টেজের উপর নির্ভর করে মোটামুটি বড় সীমার মধ্যে পরিবর্তিত হয়।
যদি সেলটি সর্বোচ্চ স্রোতে স্রাব করা হয় এবং তদ্ব্যতীত, বাধা ছাড়াই, এটি অনেক কম ক্ষমতা দেবে। বিপরীতে, যখন একই কোষটি নিম্ন প্রবাহে এবং ঘন ঘন এবং অপেক্ষাকৃত দীর্ঘ বাধার সাথে নিঃসৃত হয়, তখন কোষটি তার সম্পূর্ণ ক্ষমতা ছেড়ে দেবে।
কোষের ক্ষমতার উপর চূড়ান্ত স্রাব ভোল্টেজের প্রভাবের জন্য, এটি মনে রাখা উচিত যে গ্যালভানিক কোষের স্রাবের সময়, এর অপারেটিং ভোল্টেজ একই স্তরে থাকে না, তবে ধীরে ধীরে হ্রাস পায়।
ইলেক্ট্রোকেমিক্যাল কোষের সাধারণ প্রকার
সর্বাধিক সাধারণ গ্যালভানিক কোষগুলি হল ম্যাঙ্গানিজ-জিঙ্ক, ম্যাঙ্গানিজ-এয়ার, এয়ার-জিঙ্ক এবং লবণ এবং ক্ষারীয় ইলেক্ট্রোলাইট সহ পারদ-জিঙ্ক সিস্টেম। লবণ ইলেক্ট্রোলাইট সহ শুষ্ক ম্যাঙ্গানিজ-জিঙ্ক কোষগুলির একটি প্রাথমিক ভোল্টেজ 1.4 থেকে 1.55 V, অপারেশনের সময়কাল সকালে 7 থেকে 340 পর্যন্ত -20 থেকে -60 এর পরিবেষ্টিত তাপমাত্রায়
ক্ষারীয় ইলেক্ট্রোলাইট সহ শুকনো জিঙ্ক-ম্যাঙ্গানিজ এবং দস্তা-বায়ু কোষগুলির ভোল্টেজ 0.75 থেকে 0.9 V এবং একটি অপারেটিং সময় 6 ঘন্টা থেকে 45 ঘন্টা।
শুষ্ক পারদ-দস্তা কোষগুলির 1.22 থেকে 1.25 V এর প্রারম্ভিক ভোল্টেজ এবং 24 ঘন্টা থেকে 55 ঘন্টার একটি অপারেটিং সময় থাকে।
শুষ্ক পারদ-দস্তা কোষে 30 মাস পর্যন্ত দীর্ঘতম গ্যারান্টিযুক্ত শেলফ লাইফ থাকে।

ব্যাটারি
ব্যাটারি এগুলি হল সেকেন্ডারি ইলেক্ট্রোকেমিক্যাল কোষ৷ গ্যালভানিক কোষগুলির বিপরীতে, সমাবেশের পরপরই ব্যাটারিতে কোনও রাসায়নিক প্রক্রিয়া ঘটে না৷
ব্যাটারির জন্য বৈদ্যুতিক চার্জের গতিবিধির সাথে যুক্ত রাসায়নিক বিক্রিয়া শুরু করার জন্য, এটির ইলেক্ট্রোডের (এবং আংশিকভাবে ইলেক্ট্রোলাইটের) রাসায়নিক গঠন যথাযথভাবে পরিবর্তন করা প্রয়োজন।ইলেক্ট্রোডের রাসায়নিক সংমিশ্রণে এই পরিবর্তনটি ব্যাটারির মধ্য দিয়ে প্রবাহিত বৈদ্যুতিক প্রবাহের ক্রিয়ায় ঘটে।
অতএব, একটি ব্যাটারিতে বৈদ্যুতিক প্রবাহ উৎপন্ন করার জন্য, এটিকে প্রথমে কিছু বাহ্যিক কারেন্ট উৎস থেকে সরাসরি বৈদ্যুতিক প্রবাহ দিয়ে "চার্জ" করতে হবে।
ব্যাটারিগুলি প্রচলিত গ্যালভানিক কোষগুলির থেকেও আলাদা যে, স্রাবের পরে, সেগুলি পুনরায় চার্জ করা যেতে পারে। ভাল যত্ন সহ এবং স্বাভাবিক অপারেটিং অবস্থার অধীনে, ব্যাটারি কয়েক হাজার চার্জ এবং ডিসচার্জ পর্যন্ত স্থায়ী হতে পারে। ব্যাটারি চালিত ডিভাইস
ব্যাটারি চালিত ডিভাইস
বর্তমানে, সীসা এবং ক্যাডমিয়াম-নিকেল ব্যাটারিগুলি প্রায়শই অনুশীলনে ব্যবহৃত হয়। সালফিউরিক এসিডের প্রথম দ্রবণে ইলেক্ট্রোলাইট হিসেবে কাজ করে এবং দ্বিতীয় দ্রবণে পানিতে ক্ষার। লিড-অ্যাসিড ব্যাটারিকে অ্যাসিড এবং নিকেল-ক্যাডমিয়াম-ক্ষারীয় ব্যাটারিও বলা হয়।
ব্যাটারির পরিচালনার নীতিটি ইলেক্ট্রোডগুলির মেরুকরণের উপর ভিত্তি করে তড়িৎ বিশ্লেষণের সময়... সহজতম অ্যাসিড ব্যাটারিটি নিম্নরূপ গঠন করা হয়েছে: এটি একটি ইলেক্ট্রোলাইটে নিমজ্জিত দুটি সীসা প্লেট। রাসায়নিক প্রতিস্থাপন প্রতিক্রিয়ার ফলে, প্লেটগুলি Pb + H2SO4 = PbSO4 + H2 সূত্র থেকে অনুসরণ করে, সীসা সালফেট PbSO4 এর একটি পাতলা আবরণ দিয়ে আবৃত থাকে।
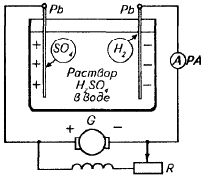
অ্যাসিড ব্যাটারি ডিভাইস
প্লেটগুলির এই অবস্থাটি একটি ডিসচার্জ হওয়া ব্যাটারির সাথে মিলে যায়। যদি ব্যাটারিটি এখন চার্জ করার জন্য চালু করা হয়, অর্থাৎ সরাসরি কারেন্ট জেনারেটরের সাথে সংযুক্ত থাকে, তবে তড়িৎ বিশ্লেষণের কারণে প্লেটগুলির মেরুকরণ শুরু হবে। ব্যাটারি চার্জ করার ফলস্বরূপ, এর প্লেটগুলি পোলারাইজড হয়, অর্থাৎ তাদের পৃষ্ঠের পদার্থ এবং একজাতীয় (PbSO4) থেকে ভিন্ন (Pb এবং PbO2) পরিবর্তন করে।
ধনাত্মক ইলেক্ট্রোড হিসাবে সীসা ডাই অক্সাইড দিয়ে লেপা একটি প্লেট এবং নেতিবাচক ইলেক্ট্রোড হিসাবে একটি পরিষ্কার সীসা প্লেট সহ ব্যাটারিটি বর্তমান উত্সে পরিণত হয়।
চার্জিংয়ের শেষে, এতে অতিরিক্ত সালফিউরিক অ্যাসিড অণুগুলির উপস্থিতির কারণে ইলেক্ট্রোলাইটের ঘনত্ব বৃদ্ধি পায়।
এটি সীসা-অ্যাসিড ব্যাটারির বৈশিষ্ট্যগুলির মধ্যে একটি: এর ইলেক্ট্রোলাইট নিরপেক্ষ থাকে না এবং ব্যাটারি অপারেশন চলাকালীন রাসায়নিক বিক্রিয়ায় অংশ নেয়।
স্রাবের শেষে, ব্যাটারির উভয় প্লেটই আবার সীসা সালফেট দিয়ে আচ্ছাদিত হয়, যার ফলস্বরূপ ব্যাটারিটি কারেন্টের উত্স হওয়া বন্ধ করে দেয়। ব্যাটারি এই অবস্থায় আনা হয় না. প্লেটগুলিতে সীসা সালফেট গঠনের কারণে, স্রাবের শেষে ইলেক্ট্রোলাইটের ঘনত্ব হ্রাস পায়। যদি ব্যাটারি চার্জ করা হয়, তাহলে এটিকে আবার ডিসচার্জ করার জন্য আবার পোলারাইজেশন ঘটতে পারে, ইত্যাদি।
কিভাবে ব্যাটারি চার্জ করবেন
ব্যাটারি চার্জ করার বিভিন্ন উপায় আছে। সবচেয়ে সহজ হল ব্যাটারির স্বাভাবিক চার্জিং, যা নিম্নরূপ করা হয়। প্রাথমিকভাবে, 5 - 6 ঘন্টার জন্য, প্রতিটি ব্যাটারির ভোল্টেজ 2.4 V এ না পৌঁছানো পর্যন্ত ডাবল স্বাভাবিক কারেন্টে চার্জ করা হয়।
স্বাভাবিক চার্জিং কারেন্ট নির্ধারণ করা হয় সূত্র Aztax = Q/16 দ্বারা
যেখানে Q - ব্যাটারির নামমাত্র ক্ষমতা, আহ।
এর পরে, চার্জিং কারেন্ট একটি স্বাভাবিক মান হ্রাস করা হয় এবং চার্জিং শেষ হওয়ার লক্ষণ না আসা পর্যন্ত 15-18 ঘন্টা চার্জিং চলতে থাকে।
আধুনিক ব্যাটারি
নিকেল-ক্যাডমিয়াম বা ক্ষারীয় ব্যাটারিগুলি সীসা ব্যাটারির চেয়ে অনেক পরে উপস্থিত হয়েছিল এবং তাদের তুলনায় রাসায়নিক প্রবাহের আরও আধুনিক উত্স।সীসা ব্যাটারির উপর ক্ষারীয় ব্যাটারির প্রধান সুবিধা হল প্লেটের সক্রিয় ভরের সাথে সম্পর্কিত তাদের ইলেক্ট্রোলাইটের রাসায়নিক নিরপেক্ষতার মধ্যে। অতএব, ক্ষারীয় ব্যাটারির স্ব-নিঃসরণ সীসা-অ্যাসিড ব্যাটারির তুলনায় উল্লেখযোগ্যভাবে কম। ক্ষারীয় ব্যাটারিগুলির পরিচালনার নীতিটি তড়িৎ বিশ্লেষণের সময় ইলেক্ট্রোডগুলির মেরুকরণের উপর ভিত্তি করে।
রেডিও সরঞ্জামগুলিকে পাওয়ার জন্য, সিল করা ক্যাডমিয়াম-নিকেল ব্যাটারি তৈরি করা হয়, যা -30 থেকে +50 OC তাপমাত্রায় কার্যকর এবং 400 - 600 চার্জ-ডিসচার্জ চক্র সহ্য করে। এই সঞ্চয়কারীগুলি কম্প্যাক্ট প্যারালেলেপিপড এবং কয়েক গ্রাম থেকে কিলোগ্রাম পর্যন্ত ওজনের ডিস্কের আকারে তৈরি করা হয়।
নিকেল-হাইড্রোজেন ব্যাটারিগুলি স্বায়ত্তশাসিত বস্তুকে শক্তি দেওয়ার জন্য উত্পাদিত হয়। নিকেল-হাইড্রোজেন ব্যাটারির নির্দিষ্ট শক্তি হল 50 — 60 Wh kg-1।




