ইলেক্ট্রোলাইটে বৈদ্যুতিক প্রবাহ
ইলেক্ট্রোলাইটে বৈদ্যুতিক প্রবাহ সর্বদা পদার্থের স্থানান্তরের সাথে সম্পর্কিত। ধাতু এবং সেমিকন্ডাক্টরগুলিতে, উদাহরণস্বরূপ, যখন তাদের মধ্য দিয়ে কারেন্ট যায় তখন পদার্থ স্থানান্তরিত হয় না, কারণ এই মিডিয়াগুলিতে ইলেকট্রন এবং গর্তগুলি বর্তমান বাহক, কিন্তু ইলেক্ট্রোলাইটে তারা স্থানান্তরিত হয়। এর কারণ ইলেক্ট্রোলাইটে, পদার্থের ইতিবাচক এবং নেতিবাচকভাবে চার্জযুক্ত আয়নগুলি বিনামূল্যে চার্জের বাহক হিসাবে কাজ করে, ইলেকট্রন বা ছিদ্র নয়।
অনেক ধাতুর গলিত যৌগ, সেইসাথে কিছু কঠিন পদার্থ ইলেক্ট্রোলাইটের অন্তর্গত। তবে এই ধরণের কন্ডাক্টরগুলির প্রধান প্রতিনিধি, যা প্রযুক্তিতে ব্যাপকভাবে ব্যবহৃত হয়, হ'ল অজৈব অ্যাসিড, ঘাঁটি এবং লবণের জলীয় দ্রবণ।
পদার্থ, যখন একটি বৈদ্যুতিক প্রবাহ ইলেক্ট্রোলাইট মাধ্যমের মধ্য দিয়ে যায়, তখন ইলেক্ট্রোডগুলিতে মুক্তি পায়। এই ঘটনা বলা হয় তড়িৎ বিশ্লেষণ… যখন একটি বৈদ্যুতিক প্রবাহ ইলেক্ট্রোলাইটের মধ্য দিয়ে যায়, তখন পদার্থের ধনাত্মক এবং ঋণাত্মক চার্জযুক্ত আয়ন একই সাথে বিপরীত দিকে চলে।
ঋণাত্মকভাবে চার্জ করা আয়ন (অ্যায়ন) বর্তমান উৎসের ধনাত্মক ইলেক্ট্রোডে (অ্যানোড) এবং ধনাত্মক চার্জযুক্ত আয়ন (কেশন) তার ঋণাত্মক মেরুতে (ক্যাথোড) ছুটে যায়।
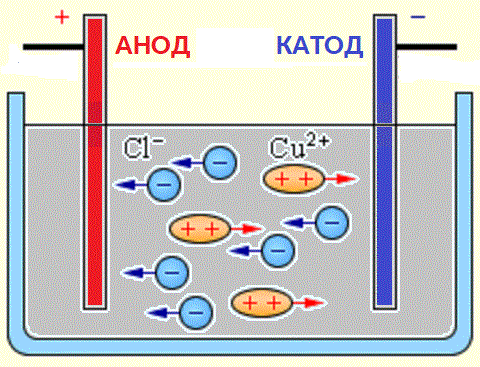
অ্যাসিড, ঘাঁটি এবং লবণের জলীয় দ্রবণে আয়নগুলির উত্স হল নিরপেক্ষ অণু, যার কিছু একটি প্রয়োগিত বৈদ্যুতিক শক্তির ক্রিয়ায় বিভক্ত হয়। নিরপেক্ষ অণুর বিভক্তির এই ঘটনাকে বলা হয় ইলেক্ট্রোলাইটিক ডিসোসিয়েশন। উদাহরণস্বরূপ, কপার ক্লোরাইড CuCl2 জলীয় দ্রবণে ক্লোরাইড আয়ন (ঋণাত্মক চার্জযুক্ত) এবং তামা (ধনাত্মক চার্জযুক্ত) মধ্যে বিয়োজনে পচে যায়।
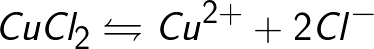
যখন ইলেক্ট্রোডগুলি একটি বর্তমান উত্সের সাথে সংযুক্ত থাকে, তখন বৈদ্যুতিক ক্ষেত্রটি একটি দ্রবণে বা গলে যাওয়া আয়নের উপর কাজ করতে শুরু করে, কারণ ক্লোরিন অ্যানয়নগুলি অ্যানোডে (ধনাত্মক ইলেক্ট্রোড) এবং তামার ক্যাথোডে (নেতিবাচক ইলেক্ট্রোড) চলে যায়।
নেতিবাচক ইলেক্ট্রোডে পৌঁছালে, ধনাত্মক চার্জযুক্ত তামার আয়নগুলি ক্যাথোডে অতিরিক্ত ইলেকট্রন দ্বারা নিরপেক্ষ হয় এবং ক্যাথোডে জমা হওয়া নিরপেক্ষ পরমাণুতে পরিণত হয়। ধনাত্মক ইলেক্ট্রোডে পৌঁছে, নেতিবাচক চার্জযুক্ত ক্লোরিন আয়নগুলি অ্যানোডের ইতিবাচক চার্জের সাথে মিথস্ক্রিয়া চলাকালীন প্রতিটি একটি ইলেকট্রন দান করে। এই ক্ষেত্রে, গঠিত নিরপেক্ষ ক্লোরিন পরমাণু জোড়ায় জোড়ায় মিলিত হয়ে Cl2 অণু তৈরি করে এবং ক্লোরিন গ্যাস বুদবুদ আকারে অ্যানোডে নির্গত হয়।
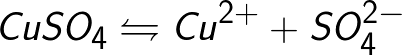
প্রায়শই, ইলেক্ট্রোলাইসিস প্রক্রিয়াটি বিচ্ছিন্নকরণ পণ্যগুলির মিথস্ক্রিয়া দ্বারা অনুষঙ্গী হয় (এটিকে সেকেন্ডারি বিক্রিয়া বলা হয়), যখন ইলেক্ট্রোডগুলিতে প্রকাশিত পচন পণ্যগুলি দ্রাবকের সাথে বা সরাসরি ইলেক্ট্রোড উপাদানের সাথে যোগাযোগ করে। উদাহরণস্বরূপ, কপার সালফেটের (কপার সালফেট — CuSO4) এর জলীয় দ্রবণের ইলেক্ট্রোলাইসিস নিন।এই উদাহরণে, ইলেক্ট্রোডগুলি তামা দিয়ে তৈরি হবে।
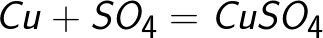
কপার সালফেট অণু বিচ্ছিন্ন হয়ে একটি ধনাত্মক চার্জযুক্ত কপার আয়ন Cu + এবং একটি ঋণাত্মক চার্জযুক্ত সালফেট আয়ন SO4- গঠন করে। নিরপেক্ষ তামার পরমাণুগুলি ক্যাথোডে একটি কঠিন জমা হিসাবে জমা হয়। এইভাবে, রাসায়নিকভাবে বিশুদ্ধ তামা পাওয়া যায়।
সালফেট আয়ন ধনাত্মক ইলেক্ট্রোডে দুটি ইলেকট্রন দান করে এবং নিরপেক্ষ র্যাডিকাল SO4 হয়ে যায়, যা তামার অ্যানোডের (সেকেন্ডারি অ্যানোড বিক্রিয়া) সাথে সাথে প্রতিক্রিয়া করে। অ্যানোডে প্রতিক্রিয়া পণ্য হল তামা সালফেট, যা দ্রবণে যায়।
এটি দেখা যাচ্ছে যে যখন একটি বৈদ্যুতিক প্রবাহ তামার সালফেটের জলীয় দ্রবণের মধ্য দিয়ে যায়, তখন তামার অ্যানোডটি ধীরে ধীরে দ্রবীভূত হয় এবং তামা ক্যাথোডের উপর ক্ষরণ করে। এই ক্ষেত্রে, তামা সালফেটের জলীয় দ্রবণের ঘনত্ব পরিবর্তন হয় না।
1833 সালে, ইংরেজ পদার্থবিদ মাইকেল ফ্যারাডে, পরীক্ষামূলক কাজের সময়, তড়িৎ বিশ্লেষণের আইন প্রতিষ্ঠা করেছিলেন, যা এখন তার নামে নামকরণ করা হয়েছে।
ফ্যারাডে আইন আপনাকে ইলেক্ট্রোলাইসিসের সময় ইলেক্ট্রোডগুলিতে প্রকাশিত প্রাথমিক পণ্যগুলির পরিমাণ নির্ধারণ করতে দেয়। আইনটি নিম্নলিখিত বলে: "ইলেক্ট্রোলাইসিসের সময় ইলেক্ট্রোডে প্রকাশিত পদার্থের ভর m ইলেক্ট্রোলাইটের মধ্য দিয়ে যাওয়া চার্জ Q-এর সরাসরি সমানুপাতিক।"
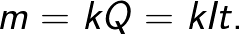
এই সূত্রের সমানুপাতিকতা ফ্যাক্টর k কে ইলেক্ট্রোকেমিক্যাল সমতুল্য বলা হয়।
তড়িৎ বিশ্লেষণের সময় ইলেক্ট্রোডে যে পদার্থটি নির্গত হয় তার ভর এই ইলেক্ট্রোডে আসা সমস্ত আয়নের মোট ভরের সমান:
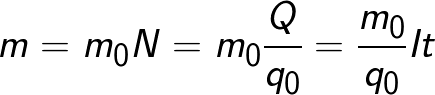
সূত্রটিতে একটি আয়নের চার্জ q0 এবং ভর m0 রয়েছে, সেইসাথে ইলেক্ট্রোলাইটের মধ্য দিয়ে যাওয়া চার্জ Q রয়েছে। N হল সেই আয়নগুলির সংখ্যা যা ইলেক্ট্রোলাইটের মধ্য দিয়ে যাওয়ার সময় ইলেক্ট্রোডে এসেছিল।তাই, m0 আয়নের ভরের সাথে এর চার্জ q0 এর অনুপাতকে k এর তড়িৎ রাসায়নিক সমতুল্য বলা হয়।
যেহেতু একটি আয়নের চার্জ সাংখ্যিকভাবে পদার্থের ভ্যালেন্স এবং প্রাথমিক চার্জের গুণফলের সমান, তাই রাসায়নিক সমতুল্যকে নিম্নলিখিত আকারে উপস্থাপন করা যেতে পারে:
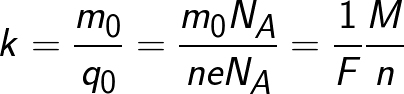
যেখানে: Na হল অ্যাভোগাড্রোর ধ্রুবক, M হল পদার্থের মোলার ভর, F হল ফ্যারাডে এর ধ্রুবক।
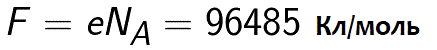
প্রকৃতপক্ষে, ফ্যারাডে ধ্রুবককে চার্জের পরিমাণ হিসাবে সংজ্ঞায়িত করা যেতে পারে যা ইলেক্ট্রোলাইটের মধ্য দিয়ে যেতে হবে ইলেক্ট্রোডের এক মোল একক পদার্থকে মুক্ত করতে। ফ্যারাডে এর তড়িৎ বিশ্লেষণের সূত্রটি তখন রূপ নেয়:
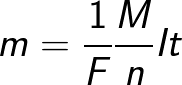
ইলেক্ট্রোলাইসিসের ঘটনাটি আধুনিক উত্পাদনে ব্যাপকভাবে ব্যবহৃত হয়। উদাহরণস্বরূপ, অ্যালুমিনিয়াম, তামা, হাইড্রোজেন, ম্যাঙ্গানিজ ডাই অক্সাইড এবং হাইড্রোজেন পারক্সাইড ইলেক্ট্রোলাইসিস দ্বারা শিল্পভাবে উত্পাদিত হয়। অনেক ধাতু আকরিক থেকে নিষ্কাশন করা হয় এবং ইলেক্ট্রোলাইসিস (ইলেক্ট্রোরিফাইনিং এবং ইলেক্ট্রো এক্সট্র্যাকশন) দ্বারা প্রক্রিয়াজাত করা হয়।
এছাড়াও, তড়িৎ বিশ্লেষণের জন্য ধন্যবাদ, রাসায়নিক বর্তমান উত্স… ইলেক্ট্রোলাইসিস বর্জ্য জল চিকিত্সায় ব্যবহৃত হয় (ইলেক্ট্রো এক্সট্র্যাকশন, ইলেক্ট্রোকোয়াগুলেশন, ইলেক্ট্রোফ্লোটেশন)। অনেক পদার্থ (ধাতু, হাইড্রোজেন, ক্লোরিন, ইত্যাদি) ইলেক্ট্রোলাইসিস দ্বারা প্রাপ্ত হয় ইলেক্ট্রোপ্লেটিং এবং ইলেক্ট্রোপ্লেটিং এর জন্য।
আরো দেখুন:জলের ইলেক্ট্রোলাইসিস দ্বারা হাইড্রোজেন উত্পাদন — প্রযুক্তি এবং সরঞ্জাম

